
«Увидеть» токсичный белок хантингтин у людей с БГ
Новые инструменты позволяют нам «видеть» скопления токсичного белка хантингтина, которые со временем накапливаются в мозге людей с болезнью Хантингтона. Отслеживание этих скоплений может помочь нам лучше понять, как прогрессирует БГ, или как методы лечения могут замедлить или остановить БГ.

Ученые разработали инструмент, который позволяет нам «видеть» токсичные скопления белка хантингтина с помощью специальных сканеров. У людей с болезнью Хантингтона (БГ) вырабатывается токсичная форма белка хантингтина, который образует скопления в клетках их организма, накапливающиеся во время прогрессирования БГ. Отслеживание того, как эти скопления образуются с течением времени у людей с БГ, или как они изменяются, когда люди с БГ принимают различные методы лечения, может помочь нам лучше понять прогрессирование БГ и какие лекарства больше всего помогают пациентам.
Что такое эти белковые скопления?
У всех нас есть 2 копии гена хантингтина, но у людей с болезнью Хантингтона (БГ) одна из их копий имеет тип мутации, называемый повторной экспансией. Эта мутация возникает в повторяющемся участке кода ДНК гена хантингтина, в котором буквы «C», «A» и «G» повторяются снова и снова. Если у вас нет БГ, у вас будет менее ~35 повторов CAG в гене хантингтина, но для людей с БГ мутация означает, что у них будет более 35 повторов CAG в одном из их генов хантингтина.
Ген хантингтина — это рецепт, который наши клетки используют для производства белка хантингтина, поэтому, если код ДНК этого рецепта изменен, белок, который производят наши тела, также будет изменен. Белки состоят из длинных цепочек химических веществ, называемых аминокислотами, в соответствии с инструкциями, изложенными в нашей ДНК. Буквы ДНК «CAG» — это рецептурные заметки для аминокислоты глутамина. Это означает, что если число повторов CAG увеличивается, белок хантингтина будет иметь гораздо больше повторяющихся глутаминов. Молекулы белка хантингтина со слишком большим количеством глутаминов не могут правильно собираться, поэтому могут образовывать токсичные скопления.
Мы знаем об этих скоплениях уже давно, и их можно увидеть в мозге людей с БГ, когда мы смотрим в микроскоп. Однако отслеживание этих скоплений у живых пациентов было сложной задачей, и большая часть наших знаний о них получена из изучения их в образцах мозга после смерти от животных моделей БГ или пациентов, которые любезно пожертвовали свой мозг для исследований.
Зачем нам смотреть на эти надоедливые скопления?
Ученые из многих лабораторий Великобритании, Германии, Италии, Швеции и США разработали молекулярные инструменты, которые теперь позволяют нам «видеть» эти скопления у живых животных и, надеюсь, в скором времени, у пациентов с БГ. Эти инструменты связываются со скоплениями белка хантингтина и имеют химические метки, называемые радиометками, которые означают, что они загораются при просмотре с помощью ПЭТ (позитронно-эмиссионной томографии).
Этот тип молекулярных инструментов известен как ПЭТ-трассеры и используется в различных медицинских и диагностических целях, чтобы позволить врачам и исследователям визуализировать определенные части вашего тела. Различные типы трассеров можно проглатывать, вводить или вдыхать в зависимости от того, какая часть вашего тела исследуется. Как только у пациента в теле появляется ПЭТ-трассер, его сканируют, и исследуемая часть тела загорается, если там находится цель ПЭТ-трассера, потому что трассер слегка радиоактивен. Аналогичные инструменты были разработаны для изучения других заболеваний, таких как питтсбургское соединение B, которое используется для изучения аналогичных скоплений у людей с болезнью Альцгеймера.
Создание ПЭТ-трассеров, которые позволяют исследователям видеть токсичные скопления белка хантингтина, является привлекательной идеей по нескольким причинам. Во-первых, ПЭТ-сканирование можно проводить пациентам в несколько моментов времени на протяжении всей их жизни, поэтому мы можем отслеживать, как скопления накапливаются с течением времени на протяжении прогрессирования БГ. Многие из наших текущих методов изучения скоплений хантингтина в мозге пациента в настоящее время можно проводить только в самом конце заболевания на ткани после смерти.
Во-вторых, ПЭТ-сканирование — это неинвазивные процедуры, которые позволяют нам заглянуть прямо в мозг, тогда как более инвазивные процедуры, такие как измерение белка хантингтина в спинномозговой жидкости, дают только приблизительное представление о том, что, по нашему мнению, происходит в мозге. В-третьих, скопления образуются из токсичной формы белка хантингтина, поэтому ПЭТ-сканирование позволит исследователям конкретно измерять изменения этой конкретной формы мутантного хантингтина. Это отличается от большинства способов, которыми мы измеряем и анализируем хантингтин в спинномозговой жидкости или крови, которые измеряют все различные формы хантингтина, включая здоровый белок хантингтина.
Разработка первого ПЭТ-лиганда хантингтина
В августе прошлого года была опубликована ранняя версия этих инструментов под названием CHDI-180R — первый случай, когда был создан ПЭТ-трассер для белка хантингтина! Команда под руководством Селии Домингес из CHDI Foundation показала, что молекула инструмента CHDI-180R способна очень плотно связываться с токсичными скоплениями белка хантингтина в пробирке. Они также использовали CHDI-180R, чтобы показать, где находятся скопления токсичного хантингтина в образцах мозга от мышиных моделей БГ.
В мозге мышей с мутацией БГ скопления токсичного белка хантингтина можно было увидеть во многих различных областях мозга, которые, как известно, поражаются БГ, тогда как у мышей без мутации БГ эти скопления не были видны, даже если им также вводили молекулу инструмента CHDI-180R. Наконец, ученые показали, что CHDI-180R хорошо распространяется по мозгу, а также безопасен и не имеет побочных эффектов как у обезьян, так и у крыс.
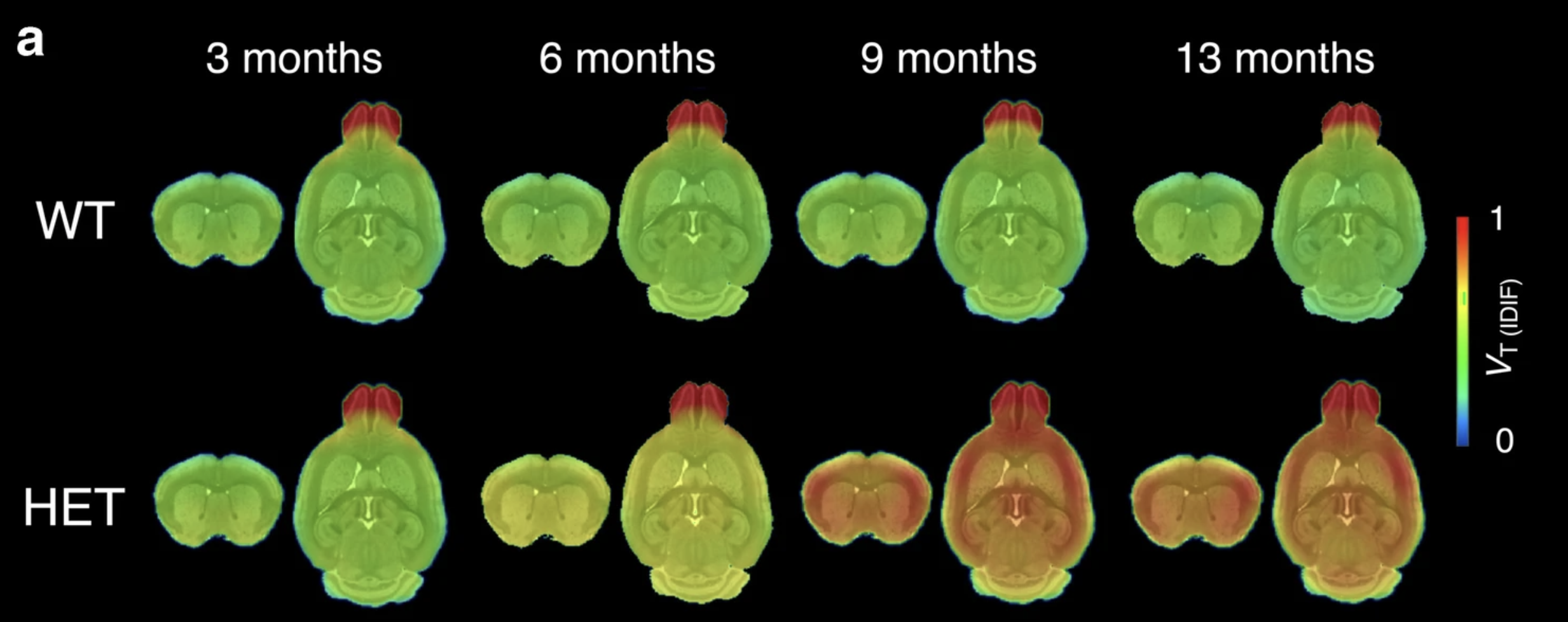
Изображение предоставлено: Bertoglio et al (2021) Eur J Nucl Med Mol Imaging
Точная настройка инструментов
Разработка ПЭТ-трассеров часто требует нескольких попыток, прежде чем будет найден оптимальный инструмент, поэтому та же международная группа ученых также разрабатывает другие версии этого трассера, чтобы иметь много резервных вариантов. Эти (надеюсь) новые и улучшенные версии молекулярного инструмента тестируются, чтобы выяснить, как они распространяются в мозге протестированных животных.
Другие заболевания, такие как болезнь Альцгеймера, также имеют белковые скопления, которые накапливаются в нервных клетках, но они состоят из других потенциально токсичных белков, таких как амилоид бета. Ученые также проверяют, насколько специфичны эти инструменты для скоплений белка хантингтина, которые накапливаются с течением времени у пациентов с БГ, по сравнению с скоплениями белков других заболеваний, таких как скопления от пациентов с болезнью Альцгеймера. Пока что результаты очень обнадеживающие, поэтому ученые теперь стремятся начать тестирование трассеров на людях.
Итак, что дальше?
Проводится клиническое исследование под названием iMagemHTT study, которое будет исследовать трассер хантингтина у людей. В исследовании будет использоваться ПЭТ/МРТ-визуализация, чтобы понять, как ПЭТ-лиганд отслеживает хантингтин в мозге. Ранее мы сообщали о некоторых обнадеживающих предварительных данных исследования фазы I этого трассера на виртуальной встрече CHDI в начале этого года. Пока что результаты обнадеживающие, поэтому они продолжают добавлять участников в исследование.
Количество скоплений хантингтина в мозге людей с БГ является хорошим биомаркером прогрессирования заболевания. Биомаркеры — это объективные измерения, которые ученые и клиницисты могут проводить для отслеживания прогрессирования БГ, что может быть важно для разработки наилучших вариантов лечения, а также для того, чтобы узнать, правильно ли работают методы лечения. Вполне возможно, что пациенты с БГ в будущем могут наблюдаться с помощью ПЭТ-сканирования с использованием этих типов инструментов.
Если ПЭТ-лиганды будут работать так, как надеются ученые, их также можно будет использовать для отслеживания снижения уровня хантингтина в мозге в будущих исследованиях. Несмотря на некоторые неудачи, снижение уровня хантингтина по-прежнему является многообещающей стратегией лечения БГ, которую преследуют Novartis, PTC Therapeutics, Wave и Uniqure, у всех из которых проводятся клинические испытания. Независимо от того, что произойдет со снижением уровня хантингтина, эти захватывающие новые инструменты дают ученым возможность — впервые в истории — отслеживать мутантный белок хантингтина во всем мозге живых пациентов с БГ, что является огромным достижением.
Мы с нетерпением ждем возможности сообщить вам больше по этой теме в ближайшее время!
Подробнее
- Визуализация агрегатов мутантного хантингтина: разработка потенциального ПЭТ-лиганда (открытый доступ)
- [11C]CHDI-626, кандидат в ПЭТ-трассеры для визуализации агрегатов мутантного хантингтина со сниженным связыванием с патологическими белками при болезни Альцгеймера (открытый доступ)
- Продольная доклиническая оценка нового радиолиганда [11C]CHDI-626 для ПЭТ-визуализации агрегатов мутантного хантингтина при болезни Хантингтона (открытый доступ)
- Фармакологическая характеристика кандидатов в трассеры для ПЭТ-визуализации, направленных на агрегаты мутантного хантингтина (открытый доступ)


